
Kalsiyum hidro karbonat nedir ve nerelerde kullanılır?
Kalsiyum hidro karbonat, Ca(HCO₃)₂ formülüyle bilinen, su ile iyi çözünme özelliğine sahip bir bileşiktir. Doğada genellikle mineral formlarda bulunur ve su arıtımı, gıda sektörü, inşaat, tarım ve medikal uygulamalarda geniş bir kullanım alanına sahiptir. Ekosistem üzerinde etkileri göz önünde bulundurulmalıdır.
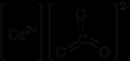
Kalsiyum Hidro Karbonat Nedir?Kalsiyum hidro karbonat, kimyasal formülü Ca(HCO₃)₂ olan bir bileşiktir. Bu bileşik, kalsiyum, hidrojen, karbon ve oksijen elementlerinin birleşiminden oluşmaktadır. Genellikle beyaz, katı bir madde olarak bulunur ve suda çözünme özelliğine sahiptir. Kalsiyum hidro karbonat, doğada genellikle mineral formunda, özellikle kalsit ve aragonit mineralleri içinde bulunur. Ayrıca, suyun içindeki kalsiyum ve karbonat iyonlarının birleşmesi sonucunda oluşan bir çökelti olarak da ortaya çıkabilir. Kalsiyum Hidro Karbonatın Özellikleri Kalsiyum hidro karbonatın bazı önemli kimyasal ve fiziksel özellikleri şunlardır:
Kalsiyum Hidro Karbonatın Kullanım Alanları Kalsiyum hidro karbonat, çeşitli endüstriyel ve günlük yaşam alanlarında geniş bir kullanım yelpazesine sahiptir. Aşağıda bu kullanım alanları detaylandırılmıştır:
Ekstra Bilgiler Kalsiyum hidro karbonat, doğada birçok yerde bulunabilir. Özellikle yeraltı su kaynaklarında ve bazı doğal göllerde, kalsiyum hidro karbonat yoğunlukla gözlemlenir. Ayrıca, bu bileşen, karstik arazilerin oluşumunda önemli bir rol oynar; suyun kalsiyum hidro karbonat içeriği yüksek olduğunda, yer altındaki kalker tabakalarını aşındırarak mağara sistemlerinin oluşumuna katkıda bulunur. Kalsiyum hidro karbonatın çevresel etkileri de dikkate alınmalıdır. Su sistemlerinde aşırı birikimi, ekosistem dengesini bozabilir ve su kalitesini olumsuz yönde etkileyebilir. Bu nedenle, kalsiyum hidro karbonat kullanımının kontrol altında tutulması önemlidir. Sonuç olarak, kalsiyum hidro karbonat, çok yönlü bir bileşik olup, birçok endüstride ve günlük yaşamda önemli bir role sahiptir. Doğadaki varlığı ve çeşitli kullanım alanları, bu bileşiğin bilimsel ve pratik açıdan ne kadar değerli olduğunu göstermektedir. |





.webp)































Kalsiyum hidro karbonatın doğada bu kadar yaygın olmasının ve birçok alanda kullanılmasının sebebi nedir? Özellikle su arıtımındaki rolü hakkında daha fazla bilgi verebilir misin? Ayrıca, ekosistem üzerindeki olumsuz etkileri nasıl kontrol altına alınabilir?
Kalsiyum bikarbonatın (Ca(HCO₃)₂) doğada yaygın olmasının temel sebebi, kireçtaşı (CaCO₃) gibi kalsiyum kaynaklarının yağmur suyu ve atmosferik karbondioksit (CO₂) ile reaksiyona girmesidir. Bu süreç, özellikle yeraltı sularında ve nehirlerde çözünmüş halde bulunmasını sağlar. Ayrıca, suyun sertliğini belirleyen ana bileşenlerden biri olması, tarım, inşaat ve endüstri gibi birçok alanda kullanılmasına olanak tanır.
Su Arıtımındaki Rolü
Kalsiyum bikarbonat, su arıtımında önemli bir rol oynar çünkü geçici su sertliğine neden olur. Bu sertlik, suyun ısıtılması veya buharlaşması sırasında kalsiyum karbonat (kireç) çökeltisi oluşturarak borularda ve ekipmanlarda birikime yol açabilir. Su arıtımında, bu bileşik genellikle kireç-soda yöntemi veya iyon değiştirme prosesleriyle uzaklaştırılır. Bu işlemler, suyun yumuşatılmasını sağlar ve korozyon, enerji kaybı gibi sorunları önler. Ayrıca, içme suyu kalitesini artırmak ve endüstriyel proseslerde verimliliği korumak için kritiktir.
Ekosistem Üzerindeki Olumsuz Etkilerinin Kontrolü
Kalsiyum bikarbonatın ekosistemdeki olumsuz etkileri, özellikle aşırı miktarlarda su kaynaklarına karışması durumunda ortaya çıkabilir; bu, suyun pH dengesini bozabilir ve su canlılarını etkileyebilir. Kontrol altına almak için şu yöntemler kullanılabilir:
- Atık su arıtma tesislerinde kimyasal çöktürme veya biyolojik işlemlerle fazla kalsiyum ve bikarbonat iyonlarının uzaklaştırılması.
- Tarımda aşırı gübre kullanımını azaltarak yeraltı sularına karışımı önlemek.
- Doğal sulak alanların korunması ve restorasyonu ile kendi kendine arıtma süreçlerini desteklemek.
- Düzenli izleme ve yasal düzenlemelerle su kalitesi standartlarının uygulanması.
Bu önlemler, çevresel dengeyi korumaya yardımcı olabilir.